Junko Muraiのこれまでのpublication (愛媛大学以前も含む)。
- Co-expression of CD30 and SLFN11 serves as a dual biomarker for the treatment of cutaneous T-cell lymphoma.
Takatoshi Shimauchi, Junko Murai, Manami Iwasaki, Pawit Phadungsaksawasdi, Toshiyuki Ojima, Kazuyasu Fujii, Tetsuya Honda
NAR cancer 7(4) zcaf037 2025年12月10.1093/narcan/zcaf037,10.1093/narcan/zcaf037
浜松医科大学皮膚科、島内先生、本田先生とのコラボ論文。皮膚T細胞リンパ腫では、CD30とSLFN11が共陽性になることが多いので、CD30を標的とするADCのpayloadはSLFN11-related drugs (TOP1/2 inhibitors)の方が理にかなっていることを示した。がん細胞特異的表面抗原がADCのバイオマーカーであるが、payloadに対するバイオマーカーも考慮に入れることで、さらなる精密医療が実現する。ADCに対して、dual biomakerという概念を初めて提唱した論文(たぶん)。
- KLHL5 Contributes to Colorectal Cancer Cell Survival by Promoting Cell Cycle Progression and Suppressing Apoptotic Cell Death
Kyosuke Habu, Yosuke Matsuoka, Hiromi Hiyoshi, Jun Nakayama, Katsuya Watanabe, Sota Tate, Tomohisa Sakaue, Junko Murai, Konomu Uno, Hirotada Nishie, Eiji Kubota, Hiromi Kataoka, Takashi Joh, Yuji Watanabe, Taro Oshikiri, Shigeki Higashiyama
Cancer Science 116(9) 2444-2456 2025年7月10.1111/cas.70108,https://onlinelibrary.wiley.com/doi/pdf/10.1111/cas.70108,10.1111/cas.70108 - PARP Inhibitors in Genitourinary Cancer: A New Paradigm Beyond Prostate Cancer.
Yohei Okuda, Taigo Kato, Yu Ishizuya, Takuji Hayashi, Yoshiyuki Yamamoto, Koji Hatano, Atsunari Kawashima, Junko Murai, Norio Nonomura
International journal of urology : official journal of the Japanese Urological Association 2025年6月9日10.1111/iju.70100,10.1111/iju.70100 - SLFN11-mediated ribosome biogenesis impairment induces TP53-independent apoptosis.
Akane Ogawa, Keiichi Izumikawa, Sota Tate, Sho Isoyama, Masaru Mori, Kohei Fujiwara, Soyoka Watanabe, Takayuki Ohga, Ukhyun Jo, Daiki Taniyama, Shojiro Kitajima, Soichiro Tanaka, Hiroshi Onji, Shun-Ichiro Kageyama, Gaku Yamamoto, Hitoshi Saito, Tomoko Yamamori Morita, Masayasu Okada, Manabu Natsumeda, Masami Nagahama, Junya Kobayashi, Akihiro Ohashi, Hiroyuki Sasanuma, Shigeki Higashiyama, Shingo Dan, Yves Pommier, Junko Murai
Molecular cell 85(5) 894-912 2025年1月30日10.1016/j.molcel.2025.01.008,10.1016/j.molcel.2025.01.008
SLFN11陽性細胞では、複製ストレスをかけた際に4−6時間程度でTP53非依存的なアポトーシスが起こるが、そのメカニズムに迫った論文。足掛け12年(本気を出してから4年)かかった論文。小川さん(当時慶應SFC学部生)泉川先生(明治薬科大学准教授)田手さん(当教室助教)がコファーストオーサー。世界と戦った達成感あり、この時のモチベを忘れずに、最後まで研究人生を貫きたい。
実験医学のcurrent topicに要約を寄稿 2025実験医学カレントトピックス
読売新聞(全国版)、毎日新聞(四国版)、Yahoo!News Japan、NHK愛媛に取り上げられた。きゃっほー。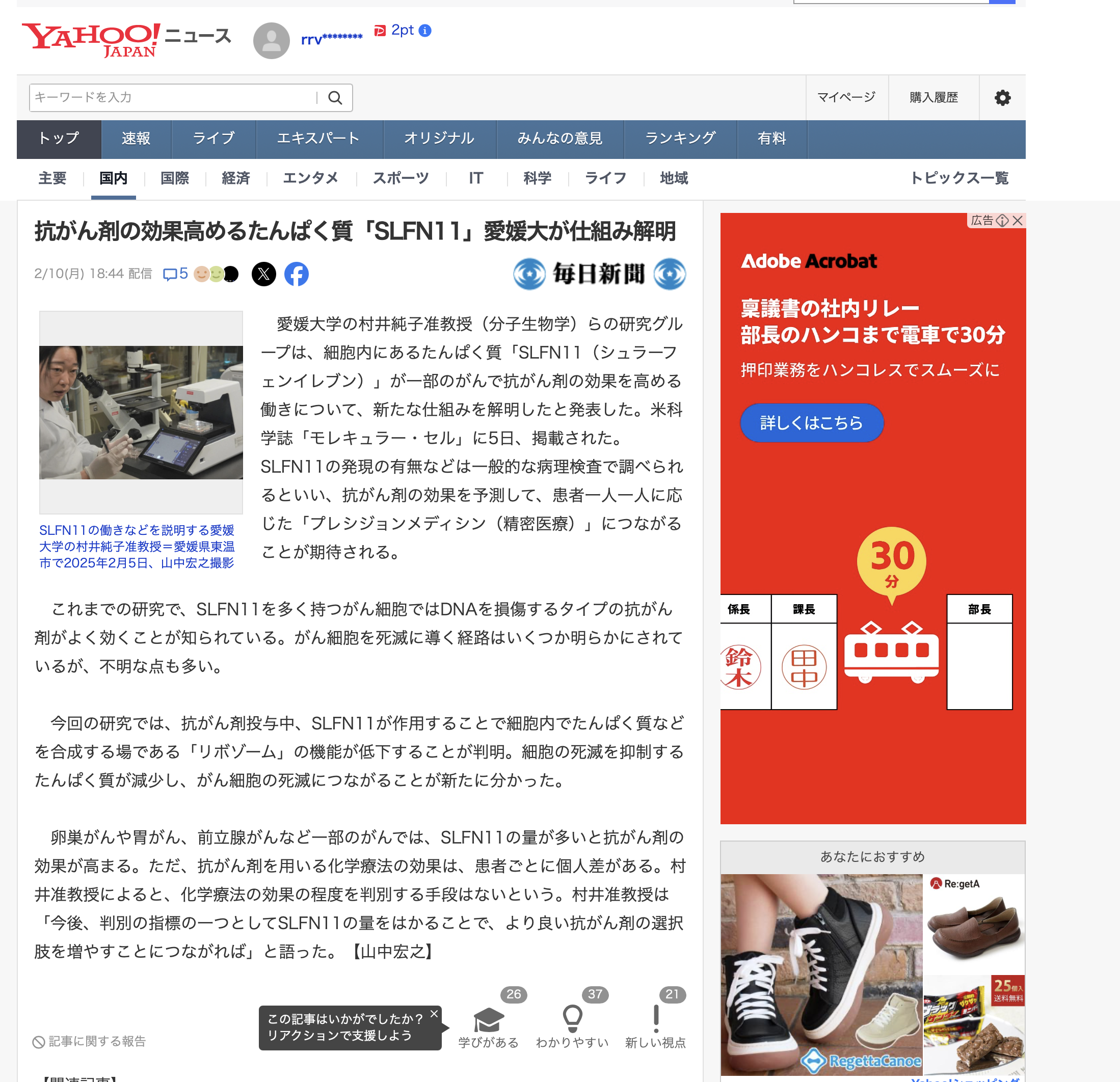
抗がん剤の効果高めるたんぱく質「SLFN11」愛媛大が仕組み解明 | 毎日新聞
- Diagnosis of Leptomeningeal Disease in Diffuse Midline Gliomas by Detection of H3F3A K27M Mutation in Circulating Tumor DNA of Cerebrospinal Fluid.
Satoshi Shibuma, Jotaro On, Manabu Natsumeda, Akihide Koyama, Haruhiko Takahashi, Jun Watanabe, Masaki Mitobe, Satoshi Nakata, Yuki Tanaka, Yoshihiro Tsukamoto, Masayasu Okada, Junichi Yoshimura, Mari Tada, Hiroshi Shimizu, Soichi Oya, Junko Murai, Kouichirou Okamoto, Hiroyuki Kawashima, Akiyoshi Kakita, Makoto Oishi
Pediatric blood & cancer e31535 2025年1月9日10.1002/pbc.31535,10.1002/pbc.31535 - Schlafen 11 further sensitizes BRCA-deficient cells to PARP inhibitors through single-strand DNA gap accumulation behind replication forks.
Hiroshi Onji, Sota Tate, Tomohisa Sakaue, Kohei Fujiwara, Shiho Nakano, Miho Kawaida, Nobuyuki Onishi, Takashi Matsumoto, Wataru Yamagami, Takashi Sugiyama, Shigeki Higashiyama, Yves Pommier, Yusuke Kobayashi, Junko Murai
Oncogene 43(32) 2475-2489 2024年7月3日10.1038/s41388-024-03094-1,10.1038/s41388-024-03094-1
PARP阻害剤は複製フォークの後方でssDNA gapを形成するが、SLFN11はそのssDNAに結合して、gapを拡げることで抗腫瘍効果を高めることを示した。BRCA変異細胞でもssDNA gapが増えるので、そこにSLFN11があるとさらにgapが増えるので、BRCAmut/SLFN11-positive腫瘍では、さらに抗腫瘍効果が高まる。筑波大学小林先生とのコラボ論文。愛媛大学において、初の大学院の指導教員を担当した恩地先生の学位論文という点でも感慨深い論文。オープンアクセスにしたところ150万円くらいかかってしまい、産婦人科教室にご迷惑をかけました。
- The crucial role of single-stranded DNA binding in enhancing sensitivity to DNA-damaging agents for Schlafen 11 and Schlafen 13.
Kohei Fujiwara, Masashi Maekawa, Yuki Iimori, Akane Ogawa, Takeshi Urano, Nobuaki Kono, Hiroyuki Takeda, Shigeki Higashiyama, Makoto Arita, Junko Murai
iScience 26(12) 108529-108529 2023年12月15日10.1016/j.isci.2023.108529,10.1016/j.isci.2023.108529
2022年にSLFN11のssDNA binding site (K652)や、ssDNA bindのために脱リン酸化されておくべきサイト(S753)が報告された。この論文では、これらのサイトがSLFN11のクロマチンリクルート、複製阻害、薬剤感受性に必須であることを、細胞レベルで示した。 さらに、SLFN11と相同性の高いSLFN13が、薬剤感受性を高めることができない理由がSLFN13のssDNA binding siteがグルタミン酸になっているからだと証明し、リジンにすることでSLFN11 likeな機能を持たせることに成功した。SLFN13の1アミノ酸変異でSLFN11 likeになるとは、クララが立った!くらいの驚きと喜びであった。慶應義塾大学薬学部大学院博士課程の3年生から「SLFN11おもろいっす、やりたいっす」とウチのラボに来てくれた藤原さんの博士論文である。SLFN11史上、後世に残ること間違いなしの秀逸論文。
- SLFN11 is a BRCA independent biomarker for the response to platinum-based chemotherapy in high-grade serous ovarian cancer and clear cell ovarian carcinoma.
Hidehiko Akashi, Nozomi Yachida, Haruka Ueda, Manako Yamaguchi, Kaoru Yamawaki, Ryo Tamura, Kazuaki Suda, Tatsuya Ishiguro, Sosuke Adachi, Yoshikazu Nagase, Yutaka Ueda, Masashi Ueda, Kaoru Abiko, Masahiro Kagabu, Tsukasa Baba, Hirofumi Nakaoka, Takayuki Enomoto, Junko Murai, Kosuke Yoshihara Molecular cancer therapeutics 23(1) 106-116 2023年9月15日10.1158/1535-7163.MCT-23-0257,10.1158/1535-7163.MCT-23-0257
新潟大学産婦人科の明石先生、吉原先生らとのコラボ論文。卵巣がんにおいて、SLFN11が高発現しているほうが、白金製剤を含む化学療法施行後のPFS,OSが長いことを、二つのコホートで共通して明らかにした。BRCA変異とは独立した指標であり、BRCA変異かつSLFN11陽性の場合、5年時点での生存率が他の群に比べ最も高かった。明石先生の学位論文。
- Schlafen 11 (SLFN11) kills cancer cells undergoing unscheduled re-replication
Junko Murai, Michele Ceribelli, Haiqing Fu, Christophe E. Redon, Ukhyun Jo, Yasuhisa Murai, Mirit I. Aladjem, Craig J. Thomas, Yves Pommier
Molecular Cancer Therapeutics 22(8) 985-995 2023年5月22日10.1158/1535-7163.MCT-22-0552/3333375/mct-22-0552.pdf,10.1158/1535-7163.mct-22-0552
SLFN11は複製ストレスを細胞にかけた時に生じるssDNAに結合して、複製ブロックを起こす。neddylation inhibitorであるMLN4924を投与した時に、CDT1の蓄積によって、M期の細胞がre-replicationを起こすことが知られているが、このre-replicationは正常複製ではなくssDNAがあちこちにできるような異常な(stressed)複製である。この論文では、SLFN11がre-replication時に生じるssDNAに結合して、re-replicationをブロックすることを示した。re-replicationは抗がん作用につながるが、SLFN11がre-replicationを止めてしまうことで、抗がん作用はさらに強くなった。つまり、SLFN11はMLN4924に対してもバイオマーカーとして機能する(ただし、度合いはCPTやプラチナに比べると弱い)。NIH時代のドラックスクリーニングプロジェクトを日本に持ち帰って、数年がかりで完成させたので自分がファースト。
- Epigenetic upregulation of Schlafen11 renders WNT- and SHH-activated medulloblastomas sensitive to cisplatin.
Satoshi Nakata, Junko Murai, Masayasu Okada, Haruhiko Takahashi, Tyler H Findlay, Kristen Malebranche, Akhila Parthasarathy, Satoshi Miyashita, Ramil Gabdulkhaev, Ilan Benkimoun, Sabine Druillennec, Sara Chabi, Eleanor Hawkins, Hiroaki Miyahara, Kensuke Tateishi, Shinji Yamashita, Shiori Yamada, Taiki Saito, Jotaro On, Jun Watanabe, Yoshihiro Tsukamoto, Junichi Yoshimura, Makoto Oishi, Toshimichi Nakano, Masaru Imamura, Chihaya Imai, Tetsuya Yamamoto, Hideo Takeshima, Atsuo T Sasaki, Fausto J Rodriguez, Sumihito Nobusawa, Pascale Varlet, Celio Pouponnot, Satoru Osuka, Yves Pommier, Akiyoshi Kakita, Yukihiko Fujii, Eric H Raabe, Charles G Eberhart, Manabu Natsumeda
Neuro-oncology 25(5) 899-912 2023年5月4日10.1093/neuonc/noac243,10.1093/neuonc/noac243
群馬大学脳外科の中田先生、新潟大学脳外科の棗田先生、NIH、ジョンスホプキンス大とのコラボ論文。脳腫瘍の一つである髄芽腫(medulloblastoma)のサブタイプ WNT-typeは、プラチナ製剤が著効しやすく、生命予後が良いことが知られていた。この論文では、WNT-typeの多くとSHH-typeの一部ではSLFN11が高発現していることを発見し、さらにSLFN11がmedulloblastomaにおいても薬剤感受性を高めていることを示した。脳神経領域の最高峰雑誌Neuro-oncologyを一本狙いで、requirementを正確に把握し、順調にアクセプトまでこぎつけた棗田先生のPIとしての手腕に感銘を受けた。
- BRCAness, Homologous Recombination Deficiencies, and Synthetic Lethality
Junko Murai, Yves Pommier
Cancer Research 83(8) 1173-1174 2023年4月14日10.1158/0008-5472.can-23-0628,https://aacrjournals.org/cancerres/article-pdf/83/8/1173/3320562/1173.pdf,10.1158/0008-5472.can-23-0628
AACRが選んだ論文(Dr. AshworshらのグループがBRCAnessを最初に提唱した論文)へのコメンタリー記事。PARP阻害剤がまだまだ熱い!
- Schlafen family member 11 indicates favorable prognosis of patients with head and neck cancer following platinum-based chemoradiotherapy
Seijiro Hamada, Satoshi Kano, Junko Murai, Takayoshi Suzuki, Nayuta Tsushima, Takatsugu Mizumachi, Masanobu Suzuki, Tsuyoshi Takashima, Daiki Taniyama, Naoya Sakamoto, Yoichiro Fujioka, Yusuke Ohba, Akihiro Homma
Frontiers in Oncology 12 978875-978875 2023年1月19日10.3389/fonc.2022.978875,https://www.frontiersin.org/articles/10.3389/fonc.2022.978875/full,10.3389/fonc.2022.978875
北海道大学耳鼻咽喉科の浜田先生らとのコラボ論文。頭頸部癌において、SLFN11がケモラジ感受性バイオマーカーとして有用であることを示した論文。頭頸部がんでは、外科的に咽頭喉頭を摘出するvs化学療法で根治を目指す、の2択を迫られることがあり、後者を選ぶ根拠としてSLFN11が有用と考えられる。まさにSLFN11の活用しどころであり、実臨床への応用を願っている。浜田先生の学位論文。
- The germline factor DDX4 contributes to the chemoresistance of small cell lung cancer cells
Christopher Noyes, Shunsuke Kitajima, Fengkai Li, Yusuke Suita, Saradha Miriyala, Shakson Isaac, Nagib Ahsan, Erik Knelson, Amir Vajdi, Tetsuo Tani, Tran C. Thai, Derek Xu, Junko Murai, Nikos Tapinos, Chiaki Takahashi, David A. Barbie, Mamiko Yajima
Communications Biology 6(1) 2023年1月18日10.1038/s42003-023-04444-7,https://www.nature.com/articles/s42003-023-04444-7.pdf,https://www.nature.com/articles/s42003-023-04444-7,10.1038/s42003-023-04444-7
研究者友達ブラウン大学矢島まみこさんとのコラボ論文。
- Metabolic clogging of mannose triggers dNTP loss and genomic instability in human cancer cells
Harada, Y., Mizote, Y., Suzuki, T., Hirayama, A., Ikeda, S., Nishida, M., Hiratsuka, T., Ueda, A., Imagawa, Y., Maeda, K., Ohkawa, Y., Murai, J., Freeze, H.H., Miyoshi, E., Higashiyama, S., Udono, H., Dohmae, N., Tahara, H., Taniguchi, N.
eLife 12 2023年10.7554/eLife.83870,http://www.scopus.com/inward/record.url?eid=2-s2.0-85164999733&partnerID=MN8TOARS,10.7554/eLife.83870 - Successful Treatment of Acute Uric Acid Nephropathy with Rasburicase in a Primary Central Nervous System Lymphoma Patient Showing a Dramatic Response to Methotrexate-Case Report.
Yoshihiro Mouri, Manabu Natsumeda, Noritaka Okubo, Taro Sato, Taiki Saito, Kohei Shibuya, Shiori Yamada, Jotaro On, Yoshihiro Tsukamoto, Masayasu Okada, Makoto Oishi, Takeyoshi Eda, Junko Murai, Hiroshi Shimizu, Akiyoshi Kakita, Yukihiko Fujii
Journal of clinical medicine 11(19) 2022年9月22日10.3390/jcm11195548,10.3390/jcm11195548 - Reconsidering the mechanisms of action of PARP inhibitors based on clinical outcomes.
Hiroshi Onji, Junko Murai
Cancer science 113(9) 2943-2951 2022年9月10.1111/cas.15477,10.1111/cas.15477
PARP阻害剤の作用機序についての総説。なぜHRPにもPARP阻害剤が使われるのか、talazoparib, olaparib, niraparibの違いなど。
- Prognostic impact of Schlafen 11 in bladder cancer patients treated with platinum-based chemotherapy.
Daiki Taniyama, Naoya Sakamoto, Tsuyoshi Takashima, Masahiko Takeda, Quoc Thang Pham, Shoichi Ukai, Ryota Maruyama, Kenji Harada, Takashi Babasaki, Yohei Sekino, Tetsutaro Hayashi, Kazuhiro Sentani, Yves Pommier, Junko Murai, Wataru Yasui
Cancer science 113(2) 784-795 2022年2月10.1111/cas.15207,10.1111/cas.15207
NIHに留学した谷山さんらとのコラボ論文。膀胱癌において世界初のSLFN11の研究。
- Schlafen 11 expression in human acute leukemia cells with gain-of-function mutations in the interferon-JAK signaling pathway
Yasuhisa Murai, Ukhyun Jo, Junko Murai, Shinsaku Fukuda, Naoko Takebe, Yves Pommier
iScience 24(10) 103173-103173 2021年10月10.1016/j.isci.2021.103173,10.1016/j.isci.2021.103173
SLFN11の発現制御はめちゃ大事ですが、JAKシグナルでSLFN11の発現が上昇することを明らかにした論文。1stの村井やすさんは、弘前大学大学院時代にNIHに留学。わずか2年で凄まじい業績をあげたが、この論文はその一つ。
- Schlafen 11 predicts response to platinum-based chemotherapy in gastric cancers.
Tsuyoshi Takashima, Daiki Taniyama, Naoya Sakamoto, Maika Yasumoto, Ryuichi Asai, Takuya Hattori, Ririno Honma, Pham Quoc Thang, Shoichi Ukai, Ryota Maruyama, Kenji Harada, Kazuya Kuraoka, Kazuaki Tanabe, Atsuo T Sasaki, Hideki Ohdan, Eiichi Morii, Junko Murai, Wataru Yasui
British journal of cancer 125(1) 65-77 2021年7月10.1038/s41416-021-01364-3,10.1038/s41416-021-01364-3
胃がん治療におけるSLFN11の有用性を明らかにした世界初の論文。(当時)広島大学分子病理学1stの高島さん、2ndの谷山さん、3rd(コレスポ)の坂本さんの見事なチームワークで、SLFN11トランスレーショナル研究の土台がこの論文でできたように思う。このお三方と出会えて本当に幸運だった。この出会いと本論文のおかげで、その後の多くのラボとのSLFN11コラボに繋がった。高島さんの修士論文その2。
- SLFN11 Inactivation Induces Proteotoxic Stress and Sensitizes Cancer Cells to Ubiquitin Activating Enzyme Inhibitor TAK-243
Yasuhisa Murai, Ukhyun Jo, Junko Murai, Lisa M. Jenkins, Shar-Yin N. Huang, Sirisha Chakka, Lu Chen, Ken Cheng, Shinsaku Fukuda, Naoko Takebe, Yves Pommier
Cancer Research 81(11) 3067-3078 2021年6月1日10.1158/0008-5472.can-20-2694,https://syndication.highwire.org/content/doi/10.1158/0008-5472.CAN-20-2694,10.1158/0008-5472.can-20-2694
SLFN11陽性細胞の方が薬剤感受性がおちるという、当初摩訶不思議だったTAK243の謎を解いた論文。SLFN11は、proteotoxic stressを抑制する方向に働くことを示した。
- SLFN11 promotes CDT1 degradation by CUL4 in response to replicative DNA damage, while its absence leads to synthetic lethality with ATR/CHK1 inhibitors.
Ukhyun Jo, Yasuhisa Murai, Sirisha Chakka, Lu Chen, Ken Cheng, Junko Murai, Liton Kumar Saha, Lisa M Miller Jenkins, Yves Pommier
Proceedings of the National Academy of Sciences of the United States of America 118(6) 2021年2月9日10.1073/pnas.2015654118,10.1073/pnas.2015654118 - De novo deoxyribonucleotide biosynthesis regulates cell growth and tumor progression in small-cell lung carcinoma
Maruyama, A., Sato, Y., Nakayama, J., Murai, J., Ishikawa, T., Soga, T., Makinoshima, H.
Scientific Reports 11(1) 2021年10.1038/s41598-021-92948-9,http://www.scopus.com/inward/record.url?eid=2-s2.0-85108953819&partnerID=MN8TOARS,10.1038/s41598-021-92948-9 - Epigenetic suppression of SLFN11 in germinal center B-cells during B-cell development.
Fumiya Moribe, Momoko Nishikori, Tsuyoshi Takashima, Daiki Taniyama, Nobuyuki Onishi, Hiroshi Arima, Hiroyuki Sasanuma, Remi Akagawa, Fathi Elloumi, Shunichi Takeda, Yves Pommier, Eiichi Morii, Akifumi Takaori-Kondo, Junko Murai
PloS one 16(1) e0237554 2021年10.1371/journal.pone.0237554,10.1371/journal.pone.0237554
ヒトの正常B細胞の分化段階におけるSLFN11の発現量を、バイオインフォ解析と、ヒト組織の胚中心などを用いて明らかにした論文。「SLFN11って正常細胞でなにしてるん?どこで発現するの?」とよく聞かれるが、その答えの一部はここにあり。preB細胞とmature B細胞(形質細胞含む)はSLFN11を高発現するが、その途中では発現が急激に下がる。胚中心では、somatic recombination, hypermutationが起こり、かつ爆発撃に細胞が増えるので、SLFN11が陽性だとマズイのかもしれない。一過性にSLFN11の発現が下がるメカニズムや生理学的意義を解明したいと思いつつ、まだできていない。1stの京都大学医学部の森部くんは当時学部生!!京大のカリキュラムであるマイコースでNIHに短期留学した時に、私とSLFN11に出会い、帰国後も独自で研究を続けたスーパー学生さん。
- Resistance to the CHK1 inhibitor prexasertib involves functionally distinct CHK1 activities in BRCA wild-type ovarian cancer.
Jayakumar Nair, Tzu-Ting Huang, Junko Murai, Brittany Haynes, Patricia S Steeg, Yves Pommier, Jung-Min Lee
Oncogene 39(33) 5520-5535 2020年8月10.1038/s41388-020-1383-4,10.1038/s41388-020-1383-4 - Immunohistochemical analysis of SLFN11 expression uncovers potential non-responders to DNA-damaging agents overlooked by tissue RNA-seq.
Tsuyoshi Takashima, Naoya Sakamoto, Junko Murai, Daiki Taniyama, Ririno Honma, Shoichi Ukai, Ryota Maruyama, Kazuya Kuraoka, Vinodh N Rajapakse, Yves Pommier, Wataru Yasui
Virchows Archiv : an international journal of pathology 478(3) 569-579 2020年5月30日10.1007/s00428-020-02840-6,10.1007/s00428-020-02840-6
広島大学分子病理学教室の、坂本先生らとのコラボ論文。SLFN11のIHCを16臓器700症例で実施した結果をまとめた論文。human genome atlasでええやん、TCGAでええやん、と思った方はぜひご一読を!SLFN11の評価にはIHCが一番なのです。SLFN11研究のバイブル的存在。1sとの高島さんは(当時)修士学生で、修士論文その1。
- Sensitivity of Mesothelioma Cells to PARP Inhibitors Is Not Dependent on BAP1 but Is Enhanced by Temozolomide in Cells With High-Schlafen 11 and Low-O6-methylguanine-DNA Methyltransferase Expression.
Daniel Rathkey, Manakamana Khanal, Junko Murai, Jingli Zhang, Manjistha Sengupta, Qun Jiang, Betsy Morrow, Christine N Evans, Raj Chari, Patricia Fetsch, Hye-Jung Chung, Liqiang Xi, Mark Roth, Armando Filie, Mark Raffeld, Anish Thomas, Yves Pommier, Raffit Hassan
Journal of thoracic oncology : official publication of the International Association for the Study of Lung Cancer 15(5) 843-859 2020年5月10.1016/j.jtho.2020.01.012,10.1016/j.jtho.2020.01.012 - BAMscale: quantification of next-generation sequencing peaks and generation of scaled coverage tracks.
Lorinc S Pongor, Jacob M Gross, Roberto Vera Alvarez, Junko Murai, Sang-Min Jang, Hongliang Zhang, Christophe Redon, Haiqing Fu, Shar-Yin Huang, Bhushan Thakur, Adrian Baris, Leonardo Marino-Ramirez, David Landsman, Mirit I Aladjem, Yves Pommier
Epigenetics & chromatin 13(1) 21-21 2020年4月22日10.1186/s13072-020-00343-x,10.1186/s13072-020-00343-x - Chromatin Remodeling and Immediate Early Gene Activation by SLFN11 in Response to Replication Stress.
Junko Murai, Hongliang Zhang, Lorinc Pongor, Sai-Wen Tang, Ukhyun Jo, Fumiya Moribe, Yixiao Ma, Masaru Tomita, Yves Pommier
Cell reports 30(12) 4137-4151 2020年3月24日10.1016/j.celrep.2020.02.117,10.1016/j.celrep.2020.02.117 - The Indenoisoquinoline TOP1 Inhibitors Selectively Target Homologous Recombination-Deficient and Schlafen 11-Positive Cancer Cells and Synergize with Olaparib.
Laetitia Marzi, Ludmila Szabova, Melanie Gordon, Zoe Weaver Ohler, Shyam K Sharan, Michael L Beshiri, Moudjib Etemadi, Junko Murai, Kathleen Kelly, Yves Pommier
Clinical cancer research : an official journal of the American Association for Cancer Research 25(20) 6206-6216 2019年10月15日10.1158/1078-0432.CCR-19-0419,10.1158/1078-0432.CCR-19-0419 - Schlafen 11 (SLFN11), a restriction factor for replicative stress induced by DNA-targeting anti-cancer therapies.
Junko Murai, Anish Thomas, Markku Miettinen, Yves Pommier
Pharmacology & therapeutics 201 94-102 2019年9月10.1016/j.pharmthera.2019.05.009,10.1016/j.pharmthera.2019.05.009 - Phosphatase 1 Nuclear Targeting Subunit, a Novel DNA Repair Partner of PARP1.
Junko Murai, Yves Pommier
Cancer research 79(10) 2460-2461 2019年5月15日10.1158/0008-5472.CAN-19-0798,10.1158/0008-5472.CAN-19-0798 - Restored replication fork stabilization, a mechanism of PARP inhibitor resistance, can be overcome by cell cycle checkpoint inhibition.
Brittany Haynes, Junko Murai, Jung-Min Lee
Cancer treatment reviews 71 1-7 2018年12月10.1016/j.ctrv.2018.09.003,10.1016/j.ctrv.2018.09.003 - Novel Fluoroindenoisoquinoline Non-Camptothecin Topoisomerase I Inhibitors.
Laetitia Marzi, Keli Agama, Junko Murai, Simone Difilippantonio, Amy James, Cody J Peer, William D Figg, Daniel Beck, Mohamed S A Elsayed, Mark Cushman, Yves Pommier
Molecular cancer therapeutics 17(8) 1694-1704 2018年8月10.1158/1535-7163.MCT-18-0028,10.1158/1535-7163.MCT-18-0028 - The evolving landscape of predictive biomarkers of response to PARP inhibitors.
Anish Thomas, Junko Murai, Yves Pommier
The Journal of clinical investigation 128(5) 1727-1730 2018年5月1日10.1172/JCI120388,10.1172/JCI120388 - Overcoming Resistance to DNA-Targeted Agents by Epigenetic Activation of Schlafen 11 (SLFN11) Expression with Class I Histone Deacetylase Inhibitors.
Sai-Wen Tang, Anish Thomas, Junko Murai, Jane B Trepel, Susan E Bates, Vinodh N Rajapakse, Yves Pommier
Clinical cancer research : an official journal of the American Association for Cancer Research 24(8) 1944-1953 2018年4月15日10.1158/1078-0432.CCR-17-0443,10.1158/1078-0432.CCR-17-0443 - Mitochondrial tyrosyl-DNA phosphodiesterase 2 and its TDP2S short isoform.
Shar-Yin N Huang, Ilaria Dalla Rosa, Stephanie A Michaels, David V Tulumello, Keli Agama, Salim Khiati, Sae Rin Jean, Simone A Baechler, Valentina M Factor, Sudhir Varma, Junko Murai, Lisa M Miller Jenkins, Shana O Kelley, Yves Pommier
EMBO reports 19(3) 2018年3月10.15252/embr.201642139,10.15252/embr.201642139 - SLFN11 Blocks Stressed Replication Forks Independently of ATR.
Junko Murai, Sai-Wen Tang, Elisabetta Leo, Simone A Baechler, Christophe E Redon, Hongliang Zhang, Muthana Al Abo, Vinodh N Rajapakse, Eijiro Nakamura, Lisa M Miller Jenkins, Mirit I Aladjem, Yves Pommier
Molecular cell 69(3) 371-384 2018年2月1日10.1016/j.molcel.2018.01.012,10.1016/j.molcel.2018.01.012 - Report on the first SLFN11 monothematic workshop: from function to role as a biomarker in cancer.
Alberto Ballestrero, Davide Bedognetti, Domenico Ferraioli, Paola Franceschelli, Sana Intidhar Labidi-Galy, Elisabetta Leo, Junko Murai, Yves Pommier, Petros Tsantoulis, Valerio Gaetano Vellone, Gabriele Zoppoli
Journal of translational medicine 15(1) 199-199 2017年10月2日10.1186/s12967-017-1296-3,10.1186/s12967-017-1296-3 - Targeting DNA repair and replication stress in the treatment of ovarian cancer.
Junko Murai
International journal of clinical oncology 22(4) 619-628 2017年8月10.1007/s10147-017-1145-7,10.1007/s10147-017-1145-7 - A subset of platinum-containing chemotherapeutic agents kills cells by inducing ribosome biogenesis stress
Peter M. Bruno, Yunpeng Liu, Ga Young Park, Junko Murai, Catherine E. Koch, Timothy J. Eisen, Justin R. Pritchard, Yves Pommier, Stephen J. Lippard, Michael T. Hemann
NATURE MEDICINE 23(4) 461-+ 2017年4月10.1038/nm.4291,10.1038/nm.4291 - ALC1/CHD1L, a chromatin-remodeling enzyme, is required for efficient base excision repair.
Masataka Tsuda, Kosai Cho, Masato Ooka, Naoto Shimizu, Reiko Watanabe, Akira Yasui, Yuka Nakazawa, Tomoo Ogi, Hiroshi Harada, Keli Agama, Jun Nakamura, Ryuta Asada, Haruna Fujiike, Tetsushi Sakuma, Takashi Yamamoto, Junko Murai, Masahiro Hiraoka, Kaoru Koike, Yves Pommier, Shunichi Takeda, Kouji Hirota
PloS one 12(11) e0188320 2017年10.1371/journal.pone.0188320,10.1371/journal.pone.0188320 - Resistance to PARP inhibitors by SLFN11 inactivation can be overcome by ATR inhibition.
Junko Murai, Ying Feng, Guoying K Yu, Yuanbin Ru, Sai-Wen Tang, Yuqiao Shen, Yves Pommier
Oncotarget 7(47) 76534-76550 2016年11月22日10.18632/oncotarget.12266,10.18632/oncotarget.12266 - In vivo evidence for translesion synthesis by the replicative DNA polymerase δ
Kouji Hirota, Masataka Tsuda, Mohiuddin, Toshiki Tsurimoto, Isadora S. Cohen, Zvi Livneh, Kaori Kobayashi, Takeo Narita, Kana Nishihara, Junko Murai, Shigenori Iwai, Guillaume Guilbaud, Julian E. Sale, Shunichi Takeda
Nucleic Acids Research 44(15) 7242-7250 2016年9月6日10.1093/nar/gkw439,10.1093/nar/gkw439 - SLFN11 Is a Transcriptional Target of EWS-FLI1 and a Determinant of Drug Response in Ewing Sarcoma.
Sai-Wen Tang, Sven Bilke, Liang Cao, Junko Murai, Fabricio G Sousa, Mihoko Yamade, Vinodh Rajapakse, Sudhir Varma, Lee J Helman, Javed Khan, Paul S Meltzer, Yves Pommier
Clinical cancer research : an official journal of the American Association for Cancer Research 21(18) 4184-93 2015年9月15日10.1158/1078-0432.CCR-14-2112,10.1158/1078-0432.CCR-14-2112 - The POLD3 subunit of DNA polymerase δ can promote translesion synthesis independently of DNA polymerase ζ.
Hirota K, Yoshikiyo K, Guilbaud G, Tsurimoto T, Murai J, Tsuda M, Phillips LG, Narita T, Nishihara K, Kobayashi K, Yamada K, Nakamura J, Pommier Y, Lehmann A, Sale JE, Takeda S
Nucleic acids research 43(3) 1671-83 2015年2月18日10.1093/nar/gkv023,10.1093/nar/gkv023 - Classification of PARP inhibitors based on PARP trapping and catalytic inhibition, and rationale for combinations with topoisomerase i inhibitors and alkylating agents
Murai, J., Pommier, Y.
Cancer Drug Discovery and Development 83 2015年10.1007/978-3-319-14151-0_10,http://www.scopus.com/inward/record.url?eid=2-s2.0-85088854670&partnerID=MN8TOARS,10.1007/978-3-319-14151-0_10 - SUMO-targeted ubiquitin ligase RNF4 plays a critical role in preventing chromosome loss
Kouji Hirota, Masataka Tsuda, Junko Murai, Tokiyo Takagi, Islam Shamima Keka, Takeo Narita, Mari Fujita, Hiroyuki Sasanuma, Junya Kobayashi, Shunichi Takeda
GENES TO CELLS 19(10) 743-754 2014年10月10.1111/gtc.12173,10.1111/gtc.12173 - Identification of novel PARP inhibitors using a cell-based TDP1 inhibitory assay in a quantitative high-throughput screening platform.
Junko Murai, Christophe Marchand, Sampada A Shahane, Hongmao Sun, Ruili Huang, Yiping Zhang, Adel Chergui, Jiuping Ji, James H Doroshow, Ajit Jadhav, Shunichi Takeda, Menghang Xia, Yves Pommier
DNA repair 21 177-82 2014年9月10.1016/j.dnarep.2014.03.006,10.1016/j.dnarep.2014.03.006 - Biochemical Assays for the Discovery of TDP1 Inhibitors
Christophe Marchand, Shar-yin N. Huang, Thomas S. Dexheimer, Wendy A. Lea, Bryan T. Mott, Adel Chergui, Alena Naumova, Andrew G. Stephen, Andrew S. Rosenthal, Ganesha Rai, Junko Murai, Rui Gao, David J. Maloney, Ajit Jadhav, William L. Jorgensen, Anton Simeonov, Yves Pommier
MOLECULAR CANCER THERAPEUTICS 13(8) 2116-2126 2014年8月10.1158/1535-7163.MCT-13-0952,10.1158/1535-7163.MCT-13-0952 - Discovery and structure-activity relationship of novel 2,3-dihydrobenzofuran-7-carboxamide and 2,3-dihydrobenzofuran-3(2H)-one-7-carboxamide derivatives as poly(ADP-ribose)polymerase-1 inhibitors.
Maulik R Patel, Aaditya Bhatt, Jamin D Steffen, Adel Chergui, Junko Murai, Yves Pommier, John M Pascal, Louis D Trombetta, Frank R Fronczek, Tanaji T Talele
Journal of medicinal chemistry 57(13) 5579-601 2014年7月10日10.1021/jm5002502,10.1021/jm5002502 - Tyrosyl-DNA-phosphodiesterases (TDP1 and TDP2).
Yves Pommier, Shar-yin N Huang, Rui Gao, Benu Brata Das, Junko Murai, Christophe Marchand
DNA repair 19 114-29 2014年7月10.1016/j.dnarep.2014.03.020,10.1016/j.dnarep.2014.03.020 - Rationale for poly(ADP-ribose) polymerase (PARP) inhibitors in combination therapy with camptothecins or temozolomide based on PARP trapping versus catalytic inhibition.
Junko Murai, Yiping Zhang, Joel Morris, Jiuping Ji, Shunichi Takeda, James H Doroshow, Yves Pommier
The Journal of pharmacology and experimental therapeutics 349(3) 408-16 2014年6月10.1124/jpet.113.210146,10.1124/jpet.113.210146 - PARP1-TDP1 coupling for the repair of topoisomerase I-induced DNA damage.
Benu Brata Das, Shar-yin N Huang, Junko Murai, Ishita Rehman, Jean-Christophe Amé, Souvik Sengupta, Subhendu K Das, Papiya Majumdar, Hongliang Zhang, Denis Biard, Hemanta K Majumder, Valérie Schreiber, Yves Pommier
Nucleic acids research 42(7) 4435-49 2014年4月10.1093/nar/gku088,10.1093/nar/gku088 - Stereospecific PARP trapping by BMN 673 and comparison with olaparib and rucaparib
J. Murai, S.-Y.N. Huang, A. Renaud, Y. Zhang, J. Ji, S. Takeda, J. Morris, B. Teicher, J.H. Doroshow, Y. Pommier
Molecular Cancer Therapeutics 13(2) 433-43 2014年2月10.1158/1535-7163.MCT-13-0803,10.1158/1535-7163.MCT-13-0803 - Differential and Common DNA Repair Pathways for Topoisomerase I- and II-Targeted Drugs in a Genetic DT40 Repair Cell Screen Panel
Yuko Maede, Hiroyasu Shimizu, Toru Fukushima, Toshiaki Kogame, Terukazu Nakamura, Tsuneharu Miki, Shunichi Takeda, Yves Pommier, Junko Murai
MOLECULAR CANCER THERAPEUTICS 13(1) 214-220 2014年1月10.1158/1535-7163.MCT-13-0551,10.1158/1535-7163.MCT-13-0551 - TDP1 repairs nuclear and mitochondrial DNA damage induced by chain-terminating anticancer and antiviral nucleoside analogs
Shar-yin N. Huang, Junko Murai, Ilaria Dalla Rosa, Thomas S. Dexheimer, Alena Naumova, William H. Gmeiner, Yves Pommier
NUCLEIC ACIDS RESEARCH 41(16) 7793-7803 2013年9月10.1093/nar/gkt483,10.1093/nar/gkt483 - Trapping of PARP1 and PARP2 by clinical PARP inhibitors
J. Murai, S.-Y.N. Huang, B.B. Das, A. Renaud, Y. Zhang, J.H. Doroshow, J. Ji, S. Takeda, Y. Pommier
Cancer Research 72(21) 5588-99 2012年11月1日10.1158/0008-5472.CAN-12-2753,10.1158/0008-5472.CAN-12-2753 - TDP2 promotes repair of topoisomerase I-mediated DNA damage in the absence of TDP1
Zhihong Zeng, Abhishek Sharma, Limei Ju, Junko Murai, Lieve Umans, Liesbeth Vermeire, Yves Pommier, Shunichi Takeda, Danny Huylebroeck, Keith W. Caldecott, Sherif F. El-Khamisy
NUCLEIC ACIDS RESEARCH 40(17) 8371-8380 2012年9月10.1093/nar/gks622,10.1093/nar/gks622 - Tyrosyl-DNA Phosphodiesterase 1 (TDP1) Repairs DNA Damage Induced by Topoisomerases I and II and Base Alkylation in Vertebrate Cells
Junko Murai, Shar-yin N. Huang, Benu Brata Das, Thomas S. Dexheimer, Shunichi Takeda, Yves Pommier
JOURNAL OF BIOLOGICAL CHEMISTRY 287(16) 12848-12857 2012年4月10.1074/jbc.M111.333963,10.1074/jbc.M111.333963 - Conditional Deletion of Bmpr1a in Differentiated Osteoclasts Increases Osteoblastic Bone Formation, Increasing Volume of Remodeling Bone in Mice
Mina Okamoto, Junko Murai, Yuuki Imai, Daisuke Ikegami, Nobuhiro Kamiya, Shigeaki Kato, Yuji Mishina, Hideki Yoshikawa, Noriyuki Tsumaki
JOURNAL OF BONE AND MINERAL RESEARCH 26(10) 2511-2522 2011年10月10.1002/jbmr.477,10.1002/jbmr.477 - Regulation of the Fanconi anemia pathway by a SUMO-like delivery network
Kailin Yang, George-Lucian Moldovan, Patrizia Vinciguerra, Junko Murai, Shunichi Takeda, Alan D. D'Andrea
GENES & DEVELOPMENT 25(17) 1847-1858 2011年9月10.1101/gad.17020911,10.1101/gad.17020911 - Regulation of the Fanconi anemia pathway by a SUMO-like delivery network
Kailin Yang, George -Lucian Moldovan, Patrizia Vinciguerra, Junko Murai, Shunichi Takeda, Alan D. D’Andrea
CANCER RESEARCH 71(17) 1847-1858 2011年9月10.1158/1538-7445.FBCR11-PR4,10.1158/1538-7445.FBCR11-PR4 - The USP1/UAF1 complex promotes double-strand break repair through homologous recombination
J. Murai, K. Yang, D. Dejsuphong, K. Hirota, S. Takeda, A.D. D’Andrea
Molecular and Cellular Biology 31(12) 2462-9 2011年6月10.1128/MCB.05058-11,10.1128/MCB.05058-11 - Insulation of the ubiquitous Rxrb promoter from the cartilage-specific adjacent gene, Col11a2
Junko Murai, Daisuke Ikegami, Mina Okamoto, Hideki Yoshikawa, Noriyuki Tsumaki
JOURNAL OF BIOLOGICAL CHEMISTRY 283(41) 27677-27687 2008年10月10.1074/jbc.M803657200,10.1074/jbc.M803657200 - Smad7 inhibits chondrocyte differentiation at multiple steps during endochondral bone formation and down-regulates p38 MAPK pathways
Takao Iwai, Junko Murai, Hideki Yoshikawa, Noriyuki Tsumaki
JOURNAL OF BIOLOGICAL CHEMISTRY 283(40) 27154-27164 2008年10月10.1074/jbc.M801175200,10.1074/jbc.M801175200 - Low-intensity pulsed ultrasound increases bone ingrowth into porous hydroxyapatite ceramic
Iwai, Takao, Harada, Yoshifumi, Imura, Koichi, Iwabuchi, Sadahiro, Murai, Junko, Hiramatsu, Kunihiko, Myoui, Akira, Yoshikawa, Hideki, Tsumaki, Noriyuki
JOURNAL OF BONE AND MINERAL METABOLISM 25(6) 392-399 2007年11月10.1007/s00774-007-0777-5,10.1007/s00774-007-0777-5 - Bone morphogenetic proteins in bone stimulate osteoclasts and osteoblasts during bone development
M Okamoto, J Murai, H Yoshikawa, N Tsumaki
JOURNAL OF BONE AND MINERAL RESEARCH 21(7) 1022-1033 2006年7月10.1359/JBMR.060411,10.1359/JBMR.060411 - Smad6/Smurf1 overexpression in cartilage delays chondrocyte hypertrophy and causes dwarfism with osteopenia
M Horiki, T Imamura, M Okamoto, M Hayashi, J Murai, A Myoui, T Ochi, K Miyazono, H Yoshikawa, N Tsumaki
JOURNAL OF CELL BIOLOGY 165(3) 433-445 2004年5月10.1083/jcb.200311015,10.1083/jcb.200311015 - Role of BMPs and Smads during endochondral bone formation
Tsumaki, N., Horiki, M., Murai, J., Yoshikawa, H.
Clinical calcium 14(7) 52-57 2004年,http://www.scopus.com/inward/record.url?eid=2-s2.0-16644372153&partnerID=MN8TOARS
