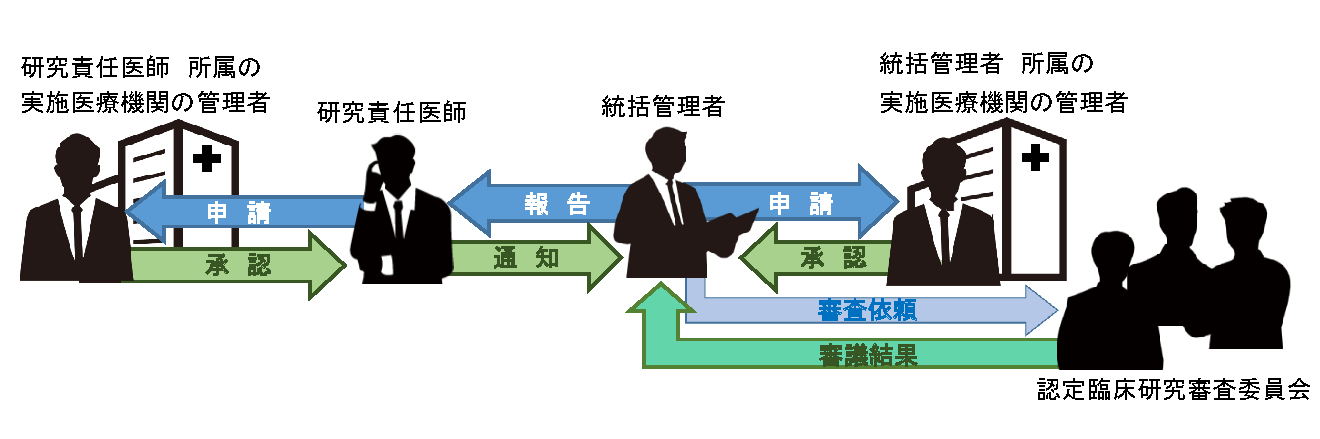
多施設共同研究(他機関代表)の実施申請手続きについて
臨床研究法における多施設共同研究において、統括管理者がCRBで審査・承認されれば自機関での審査は不要です。しかし、各研究責任医師は各所属機関にて研究実施の承認を得る必要があります。
統括管理者(または研究事務局)から承認された審査結果通知書と承認資料一式が送付され次第、速やかに実施申請の手続きをお願いします。
申請前の確認事項
下記に該当する場合は、各部門において受入可能かどうか、必ず事前に調整の上、申請してください。
●試験薬について
薬剤部に試験薬の保管・交付を依頼する場合
→ 薬剤部 治験管理室 乗松 TEL:5914
院内特殊製剤の調整を依頼する場合
→ 薬剤部 製剤室 TEL:5740
●検査について
通常の血液検査と処理が異なる等、特殊な項目がある場合
→ 検査部 高須賀 TEL:9764
1.実施申請に必要な書類の提出(提出先:研究協力課 臨床研究チーム)
・審査結果通知書…統括管理者(または研究事務局)から送付
・承認資料一式…統括管理者(または研究事務局)から送付
・実施申請書(特定臨床研究等様式05号)…書式(Excel)
※資料が不足している場合はご連絡いたします。2.実施承認書の発効
実施申請の手続きから約1~2週間後、当院病院長より実施承認書が発効されます。
3.実施承認書の提出または連絡
統括管理者(または研究事務局)から求められた場合、実施承認書を提出する(もしくは承認を得た旨メール等で連絡する。)
※新規申請/新規参加の場合…実施承認の連絡(実施承認書の提出)は必須。
※変更申請の場合…統括管理者(研究事務局)の求めに応じることになります。
多施設共同研究(他機関代表)の実施申請手続きにおける注意点
1.承認資料の提出と実施申請書の作成について
実施申請とは、CRB審査(新規審査/変更審査)承認後、実施医療機関の管理者へ研究実施の承認を得るための申請手続きになります。愛媛大学医学部附属病院では、統括管理者(または研究事務局)から送付された審査結果通知書と承認資料一式および実施申請書の提出が必要になります。実施申請書は下記【記載例】を参考に作成をお願いします。
| 実施申請 |
| 実施申請書(特定臨床研究等様式05号) |
 (様式)/ (様式)/ (記載例) (記載例) |
※「審査結果通知書」の承認資料に記載されている書類はそのままご提出ください。
別途作成する必要はありません。
※必要書類(実施申請書に項目がある書類)が送付されていない場合、統括管理者(または
研究事務局)にご確認、送付依頼をお願いします。
2.承認までの期間について
実施申請後、実施承認書の発効までは約1~2週間かかります。統括管理者(または研究事務局)より承認書の提出に期限が設けられている場合、必ずご連絡お願いいたします。
3.jRCTの登録について
多施設共同研究の場合、jRCTの登録は統括管理者(または研究事務局)が行います。研究責任医師は、実施承認書が発効された際、速やかに統括管理者(または研究事務局)へご提出をお願いいたします。
他機関で審査を受けた場合の実施申請手続きについて
愛媛大学医学部附属病院所属の研究責任医師が、愛媛大学以外のCRBにて審査・承認された場合、下記手順にそって実施申請手続きを行ってください。
1.実施申請に必要な書類の提出(提出先:研究協力課 臨床研究チーム)
・審査結果通知書
・承認資料一式
・実施申請書(特定臨床研究等様式05号)…書式(Excel)
※資料が不足している場合はご連絡いたします。2.実施承認書の発効
実施申請の手続きから約1~2週間後、当院病院長より実施承認書が発効されます。
3.jRCTの登録
実施承認書が発効された後、jRCTで実施計画の情報を登録することになります。
(申請者が統括管理者の場合は、各研究責任医師から実施承認書もしくは実施承認の連絡を
メール等で受領し、jRCTにて実施計画の情報を更新する。
申請者が研究分担機関の研究責任医師の場合、統括管理者の求めに応じることになります。)
※jRCTの登録・利用方法 ➡ jRCT操作マニュアル【登録者編】
愛媛大学臨床研究審査委員会による審査後の実施承認について
愛媛大学医学部附属病院に所属する統括管理者は、愛媛大学臨床研究審査委員会にて審査・承認された後、下記手順にそって実施申請の手続きを行います。
※他機関所属で愛媛大学臨床研究審査委員会の審査を受けた統括管理者は、自施設の管理者に研究実施の承認を得てください。
1.CRB事務局による書類の確認
審査委員会事務局(研究協力課)は、愛媛大学臨床研究審査委員会にて審査後、承認された各資料を元に実施承認の手続きを行う。2.実施承認書の発効
実施申請の手続きから約1~2週間後、当院病院長より実施承認書が発効されます。
3.jRCTの登録
※新規申請の場合…実施承認書が発行された後、jRCTで新規申請をする。
(申請者が統括管理者の場合は、各研究責任医師から実施承認書もしくは実施承認の連絡を
メール等で受領し、jRCTにて実施計画の情報を更新する。)
※臨床研究保険への加入手続きが完了した後に登録作業を行う。
※変更申請の場合…CRB承認後、jRCTで変更申請をする。
(申請者が統括管理者の場合は、各研究責任医師へ各機関での実施承認を依頼する。)
※jRCTの登録・利用方法 ➡ jRCT操作マニュアル【登録者編】
※jRCTで届出した際、CRB事務局(研究協力課)まで通知をお願いします。
※申請者が統括管理者の場合、jRCTに公表したことを各研究責任医師へ連絡お願いします。